-La autorización 510(k) de la FDA amplía el etiquetado de MolecuLight i:X® para incluir la capacidad de identificar las regiones que contienen una carga elevada y más especies bacterianas
Nueva autorización de la FDA ilustra la utilidad de i:X para detectar de forma fiable bacterias clínicamente significativas que impiden la cicatrización de las heridas
TORONTO, 29 de junio de 2022 /PRNewswire/ — MolecuLight Inc., líder en la obtención de imágenes de fluorescencia en el punto de atención para la detección en tiempo real de heridas con cargas bacterianas elevadas, anuncia que ha recibido una ampliación de su autorización 510(k) de la FDA para la capacidad del dispositivo de obtención de imágenes MolecuLight i:X® de detectar la ubicación de cargas bacterianas elevadas (>104 CFU/g) en las heridas. El etiquetado ampliado también incluye la capacidad del dispositivo para identificar zonas de las heridas que contienen más especies bacterianas, incluidos patógenos clave de interés para los CDC que son las principales causas de la resistencia a los antimicrobianos1. Las especies detectables incluyen especies gramnegativas y grampositivas, aerobios y anaerobios. Este etiquetado ampliado se basa en un detallado análisis estadístico retrospectivo de más de 350 pacientes.

“Estamos encantados con la nueva autorización de la FDA para la capacidad de MolecuLight de determinar la localización de cargas bacterianas elevadas en las heridas, además de la capacidad de identificar regiones con más especies bacterianas de interés”, dijo Anil Amlani, consejero delegado de MolecuLight. “Médicos de todo el mundo están utilizando el dispositivo MolecuLight para visualizar regiones con cargas bacterianas clínicamente significativas y más especies de interés. Con la información en el punto de atención sobre la carga bacteriana y sus localizaciones mediante el uso de un dispositivo MolecuLight, los médicos pueden actuar inmediatamente para adaptar su limpieza, desbridamiento, estrategias antimicrobianas y tratamientos en consecuencia.”
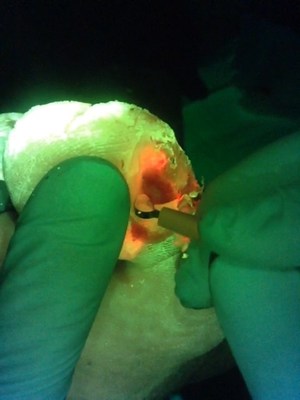
Este vídeo (cortesía de Rose Raizman) ilustra la importancia de visualizar la ubicación de la carga bacteriana elevada en una herida. En este caso, el médico utiliza MolecuLight i:X para tomar decisiones y dirigir la higiene de la herida a las zonas de fluorescencia roja. Las regiones de color rojo, que indican que la herida contiene niveles clínicamente significativos (>104 CFU/g) de carga bacteriana, son claramente visibles en la úlcera del pie diabético del paciente (véase la imagen).
Además, la FDA también ha reconocido la capacidad de MolecuLight para visualizar regiones que contienen especies bacterianas problemáticas en el punto de atención. El dispositivo MolecuLight puede utilizarse para realizar biopsias de tejido guiadas por fluorescencia en estas regiones para detectar un mayor número de patógenos de interés (definidos por los CDC como de mayor riesgo para desarrollar resistencia a los antibióticos) en comparación con las biopsias guiadas por el estándar de atención. Los CDC han identificado la resistencia a los antibióticos como “uno de los mayores retos mundiales de salud pública de nuestro tiempo “1. Las estrategias para combatir la resistencia a los antibióticos incluyen la contención de las amenazas emergentes a través de la detección temprana y la respuesta agresiva y la mejora del uso apropiado de los antibióticos a través de programas de administración de antimicrobianos. Se ha pedido que se amplíe el uso de herramientas de diagnóstico, como MolecuLight, para mejorar la precisión y la rapidez de la detección de patógenos, a fin de ayudar a mejorar la selección adecuada de antibióticos y reducir su uso innecesario1.
MolecuLight fue el primero en recibir la autorización de novo de la FDA para su plataforma de imagen MolecuLighti:X y posteriormente ha recibido otras tres autorizaciones 510(k) de la FDA para el dispositivo.
|
Referencia: |
|
|
1CDC. Antibiotic Resistance Threats in the United States, 2019. Atlanta, GA: US Department of Health and Human Services, CDC;2019 |

Acerca de MolecuLight Inc.
MolecuLight Inc. es una empresa de imágenes médicas de propiedad privada que ha desarrollado y comercializa su tecnología patentada de plataforma de imágenes fluorescentes en múltiples mercados clínicos. El conjunto de dispositivos de MolecuLight lanzados comercialmente, incluidos los sistemas de imágenes por fluorescencia MolecuLighti:X® y DX™ y sus accesorios, proporcionan dispositivos de imagen portátiles en el punto de atención para el mercado mundial del cuidado de heridas para la detección y localización en tiempo real de la carga bacteriana elevada en las heridas y para la medición digital de las heridas. Los procedimientos de MolecuLight realizados en Estados Unidos pueden beneficiarse de una vía de reembolso disponible que incluye dos códigos CPT® para el trabajo de los médicos en la realización de “imágenes de fluorescencia para la presencia, localización y carga bacteriana” y el pago de instalaciones para el Departamento de Pacientes Ambulatorios del Hospital (HOPD) y los entornos del Centro Quirúrgico Ambulatorio (ASC) a través de una asignación de Clasificación de Pago Ambulatorio (APC). La compañía también está comercializando su exclusiva tecnología de plataforma de imágenes de fluorescencia para otros mercados con necesidades no cubiertas relevantes a nivel mundial, como la seguridad alimentaria, los cosméticos de consumo y otros mercados industriales clave.
Imagen: Descarga en: https://moleculight.box.com/s/ax8758gz0f8amouhcjjvs4xzkfa9vofo
Vídeo: https://youtu.be/HKOCGBlIQj4
Rob Sandler, director de Marketing, MolecuLight Inc., T. +1.647.362.4684, rsandler@moleculight.com

