-W.L. Gore & Associates lanza GORE® SYNECOR Intraperitoneal Biomaterial en Europa, Oriente Medio y Sudáfrica
La complejidad del paciente va en aumento(1) y los cirujanos necesitan un material de alta calidad para la reparación de hernias en pacientes complejos (VHWG 2).(2)
FLAGSTAFF, Ariz., 22 de febrero de 2021 /PRNewswire/ — W. L. Gore & Associates (Gore) anunció que GORE SYNECOR Intraperitoneal Biomaterial ya está disponible en Europa, Oriente Medio y Sudáfrica. El dispositivo fue diseñado para abordar necesidades no cubiertas en la reparación compleja de hernias, proporcionando vascularización rápida3 y resistencia permanente con un perfil bajo para la reparación de hernia única y efectiva.

GORE SYNECOR Intraperitoneal Biomaterial está diseñado para facilitar su uso durante procedimientos quirúrgicos laparoscópicos, robóticos y abiertos. El material híbrido de tres capas fue aprobado y lanzado por primera vez en 2016 en los Estados Unidos y recibió la marca CE
“Esta expansión global introduce una nueva categoría de material híbrido sintético en Europa, Oriente Medio y Sudáfrica para que los cirujanos lo utilicen en la compleja reparación de hernia ventral”, dijo David Lane, líder de negocios de productos médicos generales en Gore.
Ofreciendo las últimas innovaciones a la reparación de hernias y reconstrucción de la pared abdominal
Como pionero en la categoría de malla bioabsorbible a medio plazo, Gore es persistente en la innovación de soluciones materiales para que los cirujanos tengan opciones materiales de calidad al evaluar el riesgo de complicaciones en casos complejos. GORE SYNECOR Intraperitoneal Biomaterial es flexible y conformable, con memoria para facilitar el desenrollo, el manejo y la colocación óptima. El material absorbe los fluidos corporales y no se necesita pre-remojo.
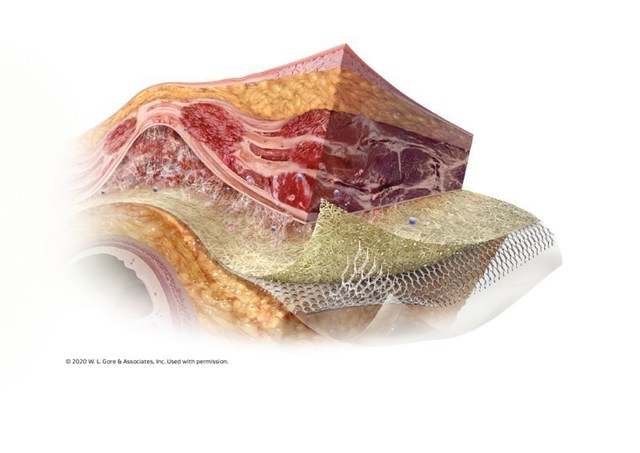
Las tres capas únicas de GORE SYNECOR Intraperitoneal Biomaterial están diseñadas para promover la vascularización rápida con material permanente mínimo3 (datos en archivo 2015; W. L. Gore & Associates, Inc; Flagstaff, AZ).
- Superficie parietal: La estructura web Gore 3D PGA:TMC genera tejido de alta calidad a través de la infiltración celular rápida. La vascularización se notifica en un plazo de siete días3 y el crecimiento de tejidos en un mes (datos en archivo 2015; W. L. Gore & Associates, Inc; Flagstaff, AZ).
- Capa media: Tejido macroporoso de densas fibras de PTFE monofilamento diseñadas con un diámetro de fibra similar a la malla ligera pero con la fuerza de la malla de peso pesado.
- Superficie visceral: La película PGA:TMC no porosa proporciona protección intra-abdominal, minimizando el riesgo de formación de adhesión al material4 (datos en archivo 2015; W. L. Gore & Associates, Inc; Flagstaff, AZ).
Para obtener más información, regístrese para asistir al Gore Complex Ventral Hernia Symposium el 16 de marzo de 2021. Registros aquí
“Estoy muy feliz de ver un nuevo material protésico, con un excelente fondo clínico y un prometedor valor añadido en la integración de tejido bajo el nuevo paradigma en la reconstrucción mínimamente invasiva de la pared abdominal,” dijo el Dr. Salvador Morales-Conde, cirujano digestivo general, Jefe de la Unidad de Innovación, Sevilla, España.
GORE SYNECOR Intraperitoneal Biomaterial es parte de una cartera de dispositivos quirúrgicos con el material sintético probado de Gore, incluyendo GORE® BIO-A® Tissue Reinforcement, GORE® SEAMGUARD® Bioabsorbable Staple Line Reinforcement, GORE-TEX® Soft Tissue Patch y GORE® DUALMESH® Biomaterial.
Para más información sobre GORE SYNECOR Intraperitoneal Biomaterial, visite https://www.goremedical.com/eu/products/synecorip
1. Mathers CD, Loncar D. Projections of global mortality and burden of disease from 2002 to 2030. PLoS Medicine 2006;3(11):e442.
2. Ventral Hernia Working Group, Breuing K, Butler CE, et al. Incisional ventral hernias: review of the literature and recommendations regarding the grading and technique of repair. Surgery 2010;148(3):544-558.
3. Crawford N. Assessment of Vascularity via Micro CT in Various Patch Devices. Flagstaff, AZ: W. L. Gore & Associates, Inc; 2016. [Final study report]. 2344TL.
4. Matthews BD. Absorbable and nonabsorbable barriers on prosthetic biomaterials for adhesion prevention after intraperitoneal placement of mesh. International Surgery 2005;90(3)Supplement:S30-S34.
Gore diseña dispositivos médicos que tratan una gama de enfermedades cardiovasculares y de otro tipo. Con más de 50 millones de dispositivos médicos implantados en el transcurso de más de 45 años, Gore se basa en su legado de mejorar los resultados de los pacientes a través de iniciativas de investigación, educación y calidad. El rendimiento del producto, la facilidad de uso y la calidad del servicio proporcionan ahorros de costes sostenibles para médicos, hospitales y aseguradoras. Gore se une al servicio con los médicos y a través de esta colaboración estamos mejorando vidas. goremedical.com
Acerca de Gore
W. L. Gore & Associates es una empresa global de ciencia de materiales dedicada a transformar industrias y mejorar vidas. Desde 1958, Gore ha resuelto complejos desafíos técnicos en entornos exigentes, desde el espacio exterior hasta los picos más altos del mundo hasta el funcionamiento interno del cuerpo humano. Con más de 11.000 asociados y una cultura fuerte y orientada al equipo, Gore genera ingresos anuales de 3.800 millones de dólares. gore.com
Es posible que los productos enumerados no estén disponibles en todos los mercados.
GORE, GORE-TEX, Together, improving life, BIO-A, DUALMESH, SEAMGUARD, SYNECOR y los diseños son marcas comerciales de W. L. Gore & Associates.



